こんにちは。Horyです。
前回の記事では化学発展の経緯を簡単に解説すると共に、ドルトンの分子説・アボガドロの分子説を説明しました。
今回の記事では原子構造が解明される経緯を解説します。
今回も頑張りましょう。
原子構造解明の経緯
原子構造解明の経緯を以下の手順に沿って解説します。
- 電子の発見 (ぶどうパンモデル)
- 原子の中身 (ラザフォードモデル)
電子の発見
1897年にトムソンが電子を発見しました。
発見の経緯としては真空管に高電圧をかけることで陰極から陽極に陰極線が放出されたことです。
中学校ではこの実験から「電流の流れは電子の流れ」というふうに習っていると思います。
陰極線の正体が電子でアリ、電子が原子の質量の1840分の1ということが分かりました。
また、トムソンはこの実験から原子の構造が以下に示すモデルになっていると考えました。
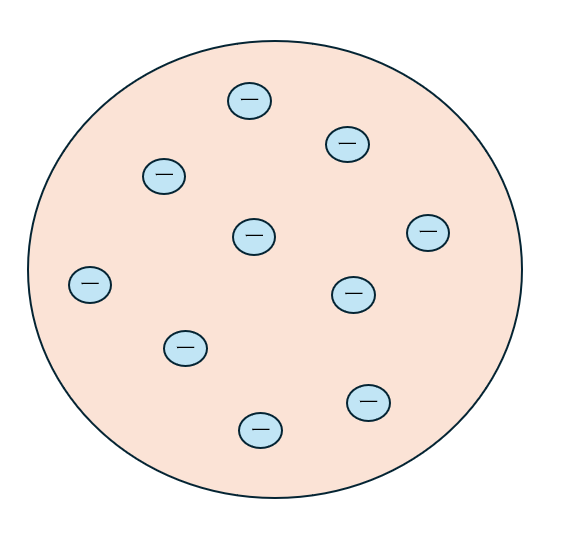
このモデルがぶどうパンに似ているということでぶどうパンモデルと呼ばれました。
- パン・・・正電荷
- 干しブドウ・・・電子
ただ、このモデルは後に登場したモデルにより否定されます。
このモデルだとダメな理由は物理の記事で説明します。
原子の中身
1900年代初頭、原子の中身について、ラザフォードは薄く伸ばした金箔にHe(ヘリウム)の原子核=α線を照射したところ、α線はほば跳ね返りませんでした。
これが示すところは、原子の中身が文字通り「スカスカ」と言うことです。また、原子はスカスカだが、質量の大部分は正電荷をもつ原子核が占めていることも分かりました。
このことから、原子は電子が原子核の周囲を周回起動するボーアモデルというモノが提唱され、現在まで使用されています。
(実際は、長岡半太郎が土星モデルを先に提唱していて、日本の方が進んでいた。ただ、立場上の問題で認められなかった)
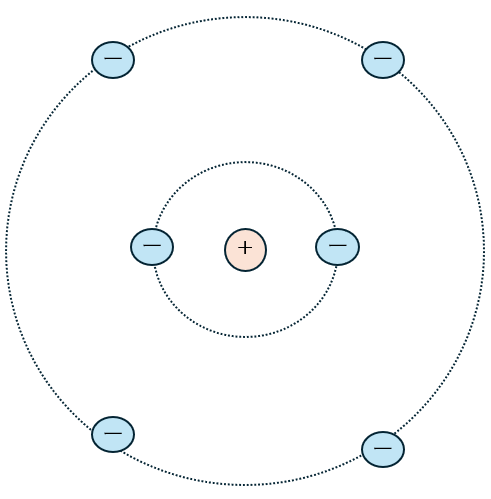
上に示す図はあくまで例です。
原子の構造
まずは、原子の基本構造についてデス。
- 原子
- 原子核
- 陽子 (正電荷)
- 中性子(電荷持たない)
- 電子殻(電子が周回軌道取る)
- 原子核
- 例外;水素原子には中性子なし
また、原子・陽子・中性子・電子の質量について・・・
- 陽子の質量は中性子の質量とほぼ同じ
- 電子の質量は中性子の1840分の1なので質量を考えるなら無視して良い
- 原子の質量は陽子と中性子の質量和に比例
また、元素記号の書き方ですが、酸素原子は普通にOと書いても良いですが、正式に書くには・・・
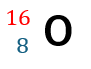
- 赤い数字(左上)・・・陽子と中性子の数の和 (質量数)
- 青い数字(左下)・・・陽子数 (原子番号)
何でこういう風に回りくどく書かないといけないかは次で解説します。
同位体の存在
同位体とは原子中の陽子数は同じですが、中性子の数が違うことで質量数が違う元素のことです。
同じ種類の原子でも質量数が違うモノがいくつもあると言うことです。ただ、陽子の数も電子の数も変わらないので性質に変化はありません。
ここで、先ほどの何故、こんな回りくどいやり方を使わなければならないかですが、原子には同位体が数千種類あります。これらに違う元素記号を一々割り当てたら収拾がつきません。
だから、原子番号を正式に書くときは左上に質量数・左下に陽子数(原子番号)を書く必要があるのです。
次回は原子における電子配置について詳しく解説します。



コメント