こんにちは。Horyです。
前回までの記事ではベンゼンへの求電子置換反応に関して、1つの置換基がベンゼンに置換する反応を解説しました。
今回の記事では2つの陽イオンのベンゼンへの置換でオルト・メタ・パラ配向性の秘密を解説します。
オルト・メタ・パラとは下の図に示すような配向性のことです。
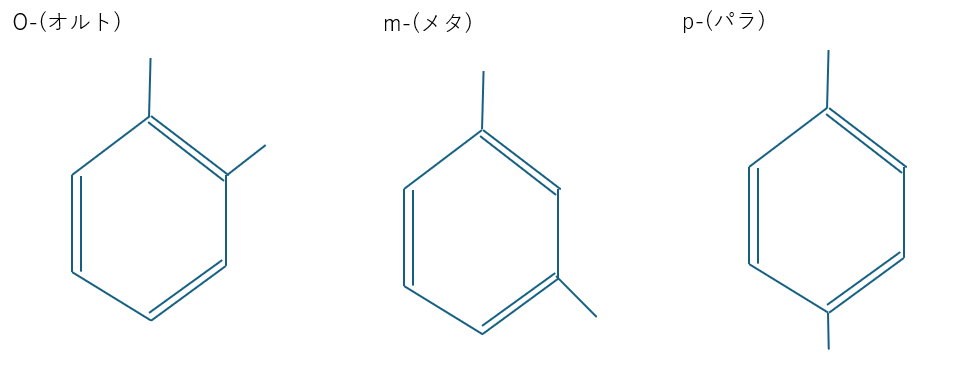
今回も頑張りましょう。
2つの陽イオンの求電子置換反応
2つの陽イオンの求電子置換反応について解説します。
具体的には一回目に置換した分子の影響を二つ目が受けることでオルト・メタ・パラのどの配向かが決まります。
具体的には2つの場合があります。
- 一分子目がアルキル基 (CH3とか) or 非共有電子対持つモノ
- 分子が電子をベンゼンに提供 (電子の吐き出し)
- ベンゼンのπ電子(二重結合の電子)と共鳴
- ベンゼンの電子が増加
- 増加した電子はオルト・パラに移動しやすい
- オルトやパラの電子密度が増加
- ベンゼンの電子を求めて陽イオンが反応
- オルト・パラの化合物が生成しやすい(オルト・パラ配向性)
- 一分子目が正電荷を持つ
- 分子がベンゼンのπ電子を引きつける (電子の吸い込み)
- ベンゼンの電子の減少
- オルト・パラの電子が移動
- オルト・パラの電子密度が低下
- 陽イオンがベンゼンの電子を求めて反応
- メタの化合物が生成しやすい(メタ配向性)
ちなみに・・・
- オルト・パラ配向・・・電子の増加(材料の増加)→反応性高い
- メタ配向・・・電子の減少(材料の減少)→反応性低い
ベンゼンのπ電子共鳴についてはこちらの記事です。
オルト・パラ配向性と官能基
オルト・パラ配向性が起こる官能基は一つ目の分子が以下の分子です(一つ目デあることに注意してください。二つ目ではありません)。
- Cl・・・クロロ
- OH・・・ヒドロキシ
- CH3・・・アルキル
- NH2・・・アミノ
ちなみに、一番反応性が強いのがフェノール性ヒドロキシ基です。ベンゼンに電子を吐き出しやすいです。
フェノキシドイオン(最強)であればなおさらです。
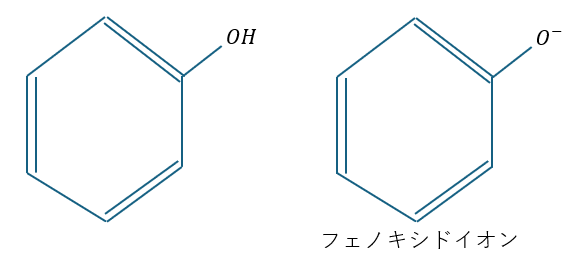
メタ配向性と置換基
メタ配向性が起こる官能基は一つ目の分子が以下の分子です(一つ目デあることに注意してください。二つ目ではありません)。
- NO2・・・ニトロ基
- SO3H・・・スルホン
- CN・・・シアン
- COOH・・・カルボキシ基
こんなところでしょうか?
頑張ってください。



コメント