こんにちは。Horyです。
今回の記事ではグループ別・元素別各論でリンに関して紹介します。
リンは15族元素の1つでアリ、同素体を多く持つ元素です。また、前回紹介した窒素と同様に肥料の原料にもなります。
今回も頑張りましょう。
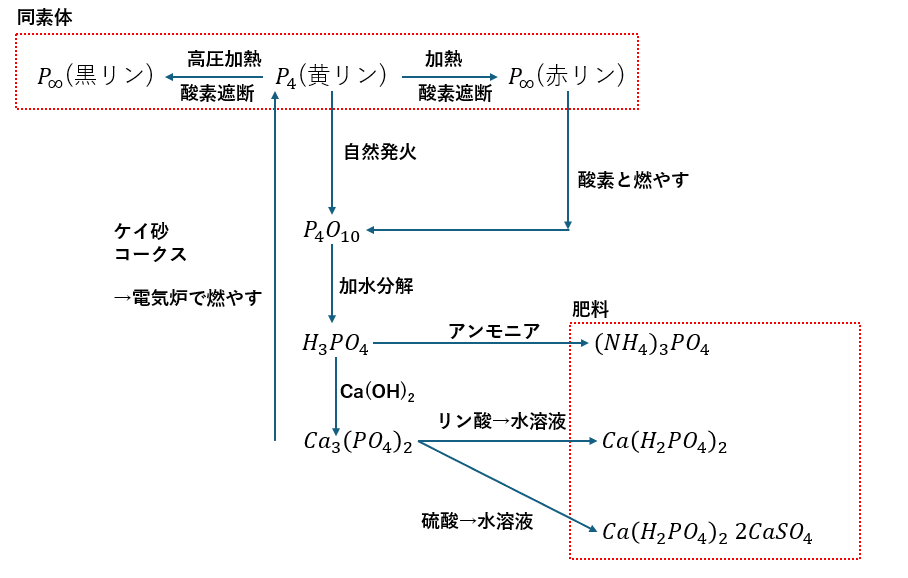
リンの同素体とその化合物
リンには3つの同素体があってそれぞれ色によって分かれています。
- リンの単体と同素体
- 黄リン(P4)・・・正四面体型で結合弱い/自然発火する/水中に保存/有毒
- 赤リン(P∞)・・・黄リンを加熱して生成/不規則/自然発火しない/無毒
- 黒リン(P∞)・・・黄リンを高圧で加熱/規則的/光沢/無毒
ちなみに、リンの単体はリン鉱石と二酸化ケイ素・コークスを混ぜて炉内で燃やすことで得られます。
化学反応式はマイナーですが以下に示すとおりです。
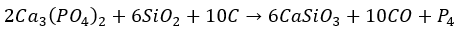
これによってできるのは黄リンです。
リンの酸化物とリン酸
リンの酸化物は十酸化四リン(P4O10)で乾燥剤としても優秀です。
ちなみにですが、P4O10は水と反応することでリン酸になります。
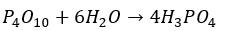
ここで、面白い事が、リン酸自体は酸性を示しますが、リン酸由来の塩の水溶液は加水分解によって塩基性になることです。
加水分解についてはこちらの記事を見といてください。
まぁ、そのうち解説しますが、リン酸は私たちの遺伝子情報のDNAとかとも大いに関係します。
リン酸の塩と肥料
リン酸の塩は化学肥料としても利用されて高校化学で頭に入れておくべき物は3つあります。
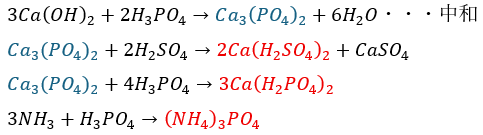
- 赤い部分・・・肥料
- 青い部分・・・リン酸カルシウム (骨の成分)
まとめ
リンとその化合物に関してまとめます。


コメント