こんにちは。Horyです。
ベンゼンに官能基をつけると性質が違う様々な有機化合物に変化することをご存じでしょうか?
今回はベンゼンが反応する原理を紹介すると共にラジカル付加反応でシクロヘキサンとかができる反応を解説します。
今回も頑張りましょう。
ベンゼンの反応
ベンゼンに官能基を付加させて別の有機化合物にしたいのであればベンゼンを反応させなければなりません。
有機化合物には3つの反応があることを以下の記事でも解説したと思いますが、念のため復習しておきます。
- ラジカル付加反応 (パッカーん反応)
- 求電子反応 (電子おねだり反応)
- 求核反応 (電子押し売り反応)
この中でどれがベンゼンと反応するかと言うことですが、反応するならベンゼンのπ電子(二重結合に関与する電子)が反応しなければなりません。
だから、電子を押し売りする求核反応は論理的に考えてもあり得なさそうです。
そのため、ベンゼンの反応はラジカル付加反応か求電子反応です(求電子反応が多く、ラジカルは少ないのでこの記事ではついでにラジカル付加反応を解説)。
上の3つの反応を図にまとめます。復習も兼ねて見ておいてください。
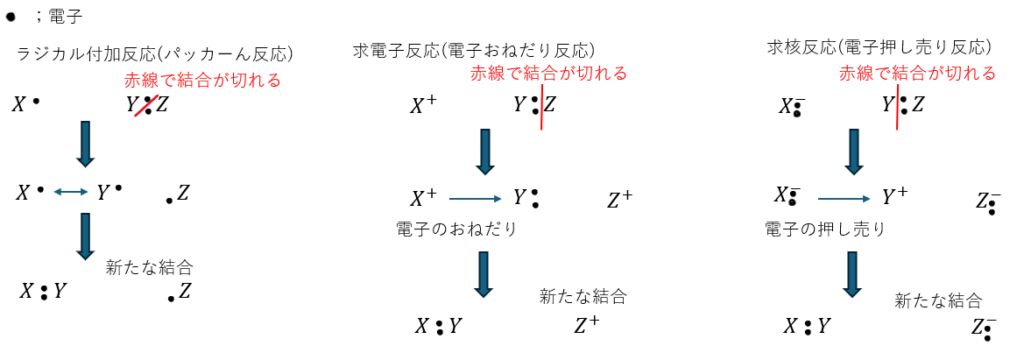
ベンゼンへのラジカル付加反応
ベンゼンへのラジカル付加反応で覚えておいた方がいいものを示します。
原理としては以下のようになります。
- ベンゼンのπ電子をHやハロゲンの不対電子が奪う
- ベンゼンの共鳴が一時的に消えて不安定に
- 安定になるためにベンゼンに大量のHやハロゲンが攻撃→ラジカル付加
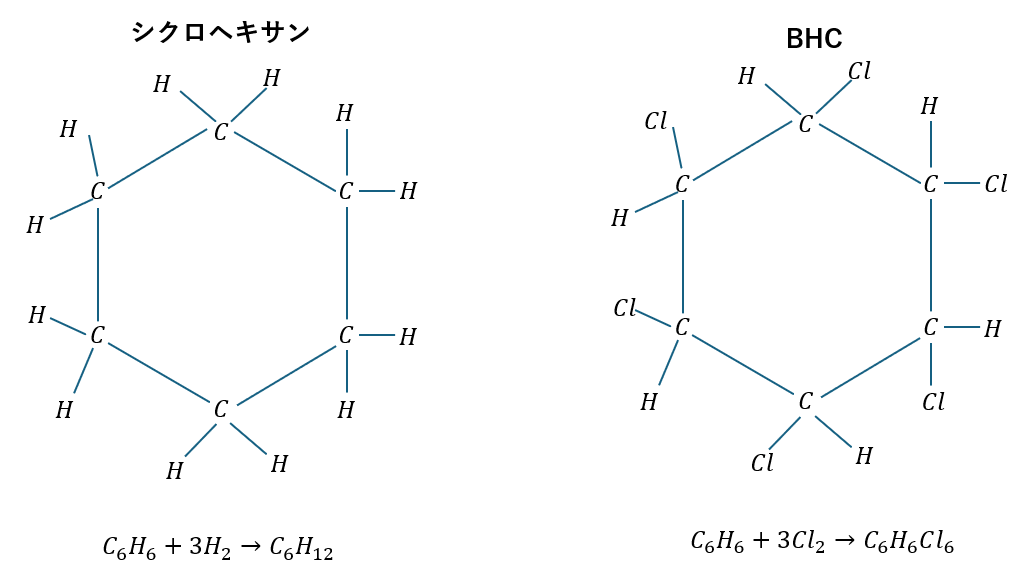
- 水素が高圧でラジカル付加反応
- →シクロヘキサンの生成
- 紫外線で塩素の反応
- →ベンゼンヘキサクロリド(BHC)の生成
ちなみに、このような場合はニッケル(Ni)やプラチナ(Pt)を触媒にすることが普通です。
ラジカル付加反応が少ない理由ですが、電子を求めて大量のHやハロゲンイオンが突撃すると言うことは陽イオン同士が反発すると言うことです。
Clなどの塩素は一価の陰イオンの形が有名ですが、無理矢理電子を引っぺがして陽イオンにもできます。
だから高圧で触媒のある条件下で反応させるのです。



コメント