こんにちは。Horyです。
今回の記事ではフェノールの製法に関する記事を書きます。
高校化学でフェノールの製法はサラッと触れられますが、その製法はめちゃくちゃ奥が深いです。
今回の記事では原理から解説します。
頑張りましょう。
フェノールの製法
フェノールもベンゼンのクロロ化やニトロ化のように一価の陰イオンで安定な元素で条件を過酷にして一価の陽イオンにすると考えられますが・・・
- OHを一価の陽イオン→無理
- OH一価の陰イオン→無理矢理反応させるしかない・・・
ヒドロキシ基を一価の陽イオンにすることは非常に困難です。
そのため、陰イオンの状態で無理矢理反応させれば・・・と思いますが、、、
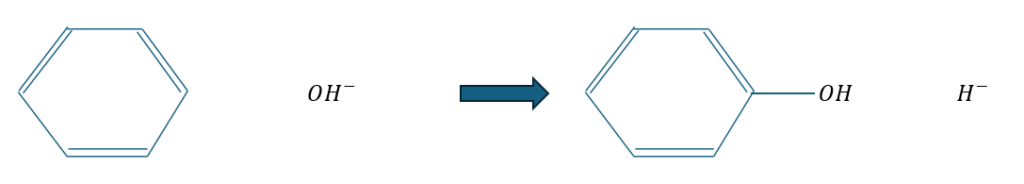
上の反応も現実的に不可能に近いです。というのも、一価の陽イオンで安定な水素が陰イオンとして存在していることです。
水素の特徴を考えてみてください。この記事でも解説しましたが、原子半径が小さい水素に2つの電子が存在することを考えてみてください。
マイナスの電荷を持った電子は反発しますよね。だから、水素の陰イオンを生成する上の反応は起こりえないです。
「困ったモノだ」と思って昔の人はフェノールを作る方法を考えたところ、「直接的にフェノールを作るのではなく、一段落はさんでフェノールを作る」という方法を思いついたのです。
どういうことかと言うと・・・
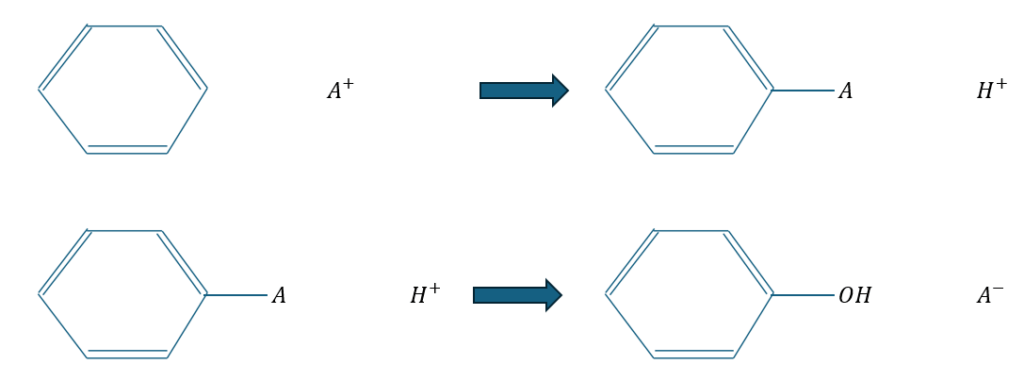
図に示すように元素Aの求電子反応を挟んでフェノールを作る方法ですが、この元素Aが陽イオンでも陰イオンでも安定するものであればフェノールを生成できると言うことです。
パッと思いつくのは・・・
- クロロ化経由でのフェノール生成
- スルホン化経由でのフェノール生成
- クメン法によるフェノール生成 (重要)
ただ、上の方法でも何とかフェノールができるというレベルです。だから、フェノールを作るときは高温・高圧という過酷な条件を課しているのです。
クロロ化経由でのフェノール生成
クロロ化経由でのフェノールの製法を紹介します。
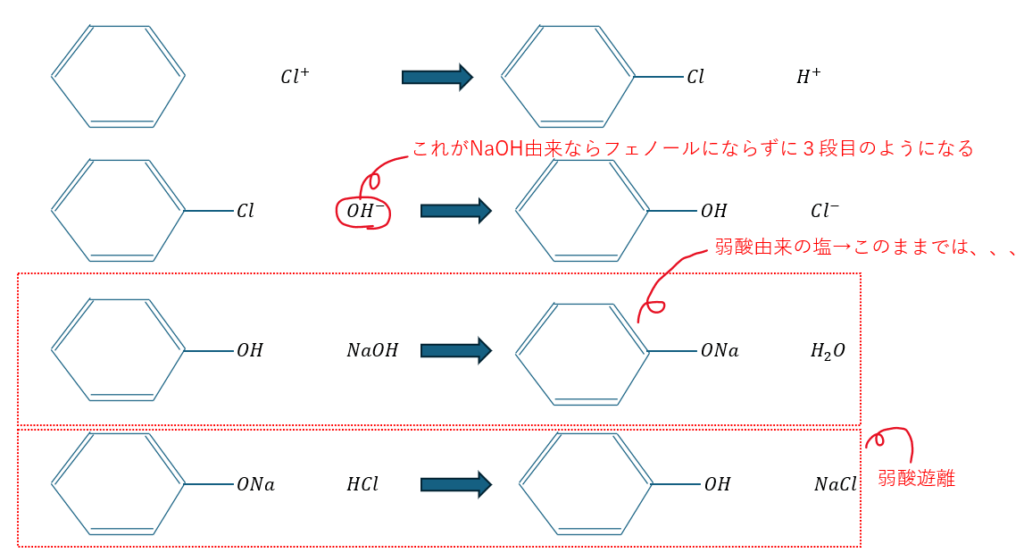
上の図の2段目のように一気にフェノールが生成されるわけではありません。
というのも、OHがNaOH由来とかであれば3段目のようにナトリウムフェノキシドが生成されます。
これを4段目にて強酸である塩酸と反応させると弱酸のフェノールが分離します(弱酸遊離反応)。
スルホン化経由でのフェノール生成
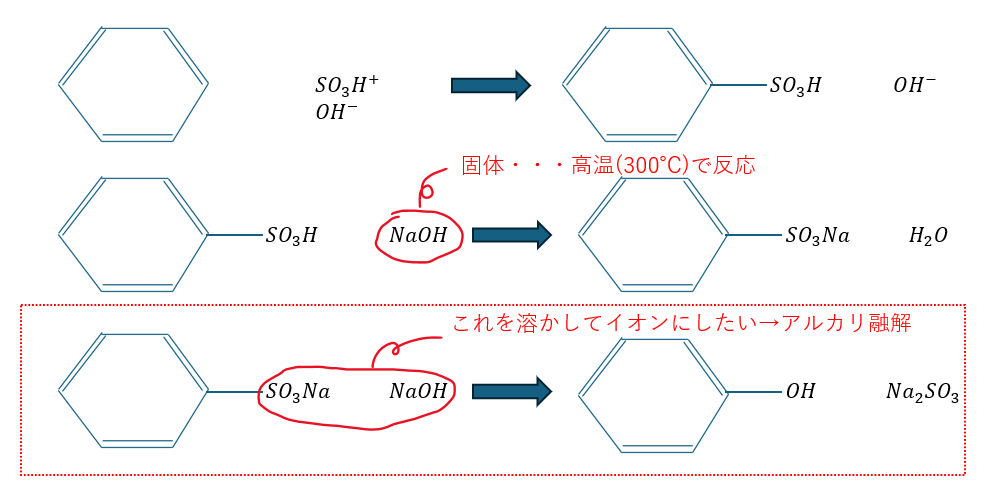
スルホン化経由でのフェノールの製法を紹介します。原理はクロロ化経由の時と同じです。
クメン法によるフェノール生成 (工業的)
クメン法でフェノールを作る方法を解説します。
昔はクロロ化やスルホン化を経由してフェノールが作られていましたが、実は問題が二点ほどあります。
- 多量のNaOH
- 過酷な条件 (アルカリ融解である以上、高温・高圧)
- →莫大なコスト
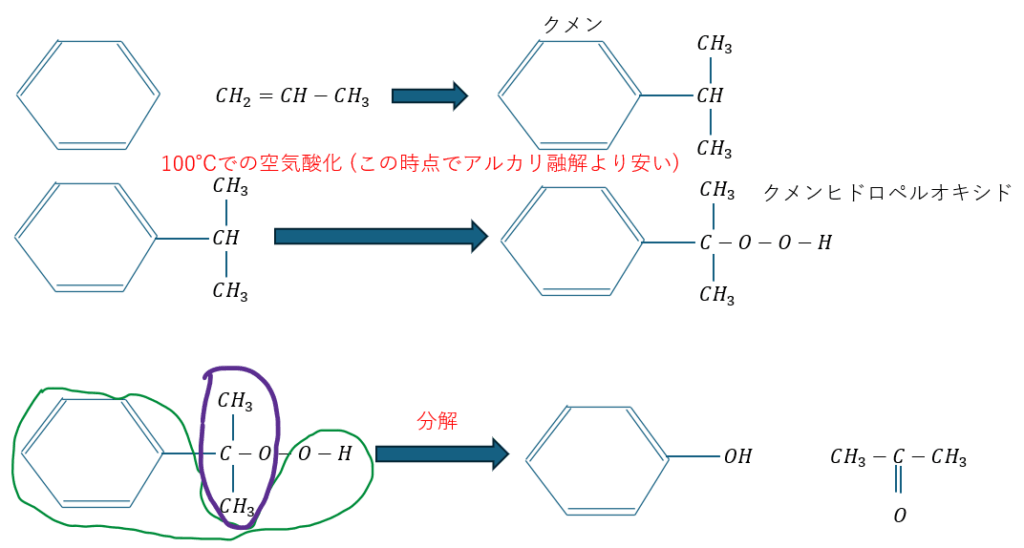
これの解決のためクメンと呼ばれる有機化合物を使います。クメン法はフェノールやアセトンを大量生産するための方法です。
図に反応方法を示します。



コメント