こんにちは。Horyです。
今回はグループ別・元素別各論でケイ素について紹介します。
前回紹介した炭素と同じ14族元素であり、日常生活でも非常に応用されている元素になります。
今回も頑張りましょう。
ケイ素の性質
ケイ素の性質を以下に示します。
- 地殻中に酸素に次いで多く含まれる
- 単体では存在せず、酸素と結合した二酸化ケイ素として存在する
- ダイアモンド型の結晶構造
- 半導体の材料/ファインセラミックスの材料
ケイ素は酸素以外にもフッ素(F)やケイ素自身とも結合しますが、結合エネルギーはSi<O<Fの順になっています。
結合エネルギーが大きい方が安定するため、地殻中では酸素と結合しています(フッ素は自然中にそこまでない)。
ケイ素の単体を得るには以下のように二酸化ケイ素とコークスを反応させます。

ケイ素と半導体について
ケイ素は半導体の材料にもなります。
そもそも、半導体とはどんな物質かというと・・・
- 導体・・・電気を通す物質(金属とか)
- 絶縁体・・・電気を通さない物質(ゴムとか)
- 半導体・・・電気を通すこともあるし、通さないこともある物質
このように、導体と絶縁体の特性を両方持つ物質が半導体と言います。
半導体が電気を流すメカニズムは以下の通りです。
- 半導体の温度上昇
- 結合が切れ始める
- 結合が切れると一部の電子が自由に動ける
- 自由に動ける電子は自由電子のようになる
- 電気が流れる
また、言葉だけでも良いですが、n型半導体とp型半導体は頭に入れておいてください(物理の記事で解説します)。
ケイ素とファインセラミックス
皆さんはファインセラミックスという言葉を聞いたことがありますでしょうか?
二酸化ケイ素をコークスと反応させて以下の物質を作ります(炉内で強熱する)。
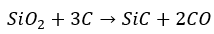
上の化学反応式の右辺にあるSiCはファインセラミックスの一種です。
ケイ素と炭素が結合して硬さ・耐熱・安定に優れていて非常に使い勝手が良いです。
ファインセラミックスは電子部品など私たちの日常生活を大きく支えています。
今回紹介したSiC以外も調べてみてください。
二酸化ケイ素からの化合物
二酸化ケイ素を起点とした化合物も日常生活で非常に多く使用されています。
- SiO2が多数結合→結晶化→光ファイバー/石英ガラス
- SiO2(ケイ砂)+Na2CO3→ソーダガラス
- ソーダガラス+ Na2CO3→ケイ酸ナトリウム(Na2SiO3)→加熱→水ガラス
- 水ガラス+塩酸→ケイ酸(H2SiO3)=ゲル=コロイド
- ケイ酸→砕く→加熱→シリカゲル・・・多孔質/水素結合→乾燥剤
- ケイ酸塩・・・ケイ素が複数の酸素と化合して陰イオン化
ここで、上の内容を図にしてみます。
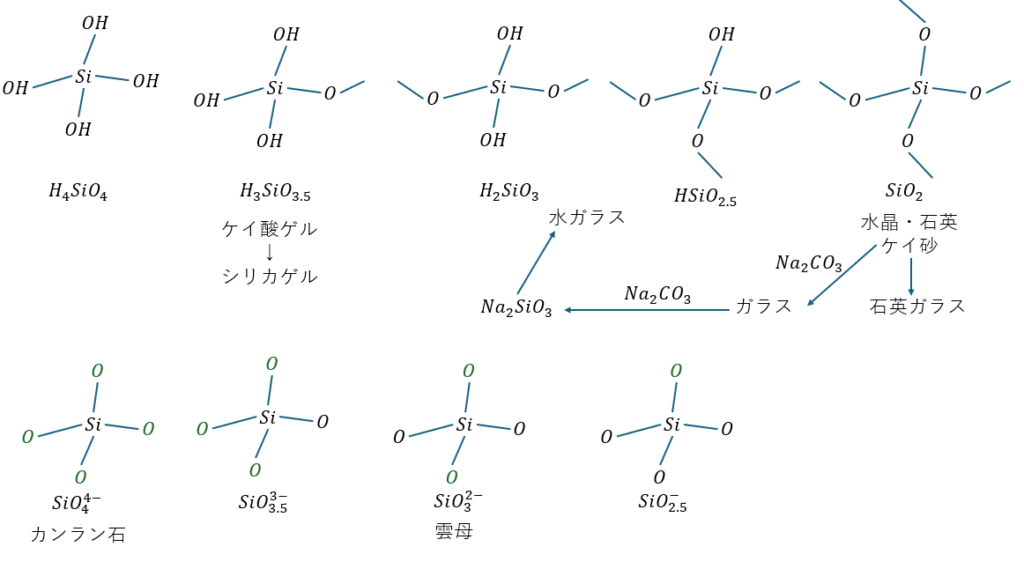
まとめ
ケイ素とその化合物をまとめます。
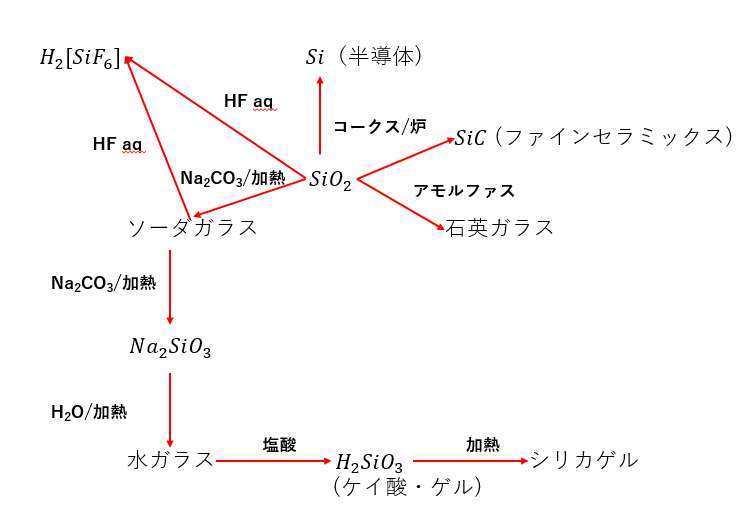



コメント