こんんちは。Horyです。
今回はグループ別・元素別各論でアルカリ土類金属に関して解説します。
アルカリ土類金属で一番大事なのはカルシウムになるので、重点的にやろうと思います。
今回も頑張りましょう。
アルカリ土類金属について・・・
アルカリ土類金属の単体とその化合物に関する内容を簡単に解説します。
- 単体について・・・
- 最外殻電子は二つ・・・アルカリ金属よりは結合強い/密度・融点も大
- Be,Mg・・・六方最密構造
- Ca・・・面心立方格子
- 石油中で保存せよ
- 水酸化物について・・・水溶液中で塩基性
- フッ化物塩について・・・フッ化バリウム以外は水に溶けにくい
- ハロゲン化物塩・・・水に溶けやすい
- 硫酸塩・・・水に溶けにくく白色沈殿
2族元素で大事になってくるのはCa(カルシウム)とMg(マグネシウム)ですが、今回はカルシウムに焦点を当てた解説を行います。
Ca(カルシウム)について・・・
カルシウムについて、学ぶべき化合物を簡単にまとめます。
- Ca・・・カルシウム→単体
- CaO・・・酸化カルシウム(生石灰)→酸化物
- Ca(OH)2・・・水酸化カルシウム(消石灰)→水酸化物
- CaCl2・・・塩化カルシウム→塩
- Ca(HCO3)2・・・炭酸水素カルシウム→塩
- CaCO3・・・炭酸カルシウム→塩
Caの単体
Ca(カルシウム)の単体を作るには塩化カルシウムの融解電解を行います。
融解電解については、ナトリウムの単体を作るときと同様で、前回の記事でも解説しました。
多量の塩化カルシウムを高温で液化して電気分解することでカルシウムの単体を得ることができます。
酸化カルシウムについて・・・
酸化カルシウムは生石灰とも呼ばれています。
作り方は2つあって・・・
- カルシウムの酸化
- 炭酸カルシウムの加熱分解

水酸化カルシウムについて・・・
水酸化カルシウムは消石灰と呼ばれていて、作り方が複数あります。
- 酸化カルシウムに水を投入
- 塩化カルシウムの水溶液電解
- カルシウムに水
上から順番に化学反応式で記述すると・・・
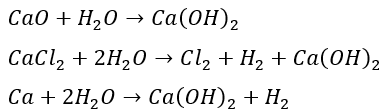
ところで、生石灰や消石灰で名前が似ていて紛らわしいと思いますが、このように覚えます。
- 生石灰・・・酸化カルシウム→水との反応で多量の発熱(生きているよう)
- 消石灰・・・水酸化カルシウム→水との反応で発熱終った(命が消えたよう)
- 石灰水・・・水酸化カルシウムを水に溶かした溶液
塩化カルシウムについて・・・
塩化カルシウムの作り方は二つありますが、どちらも弱酸遊離反応です。
弱酸遊離反応についてはこちらの記事を読んでください。
- 炭酸カルシウムに塩酸→二酸化炭素の遊離(炭酸)
- 炭酸水素カルシウムに塩酸→二酸化炭素の遊離(炭酸)
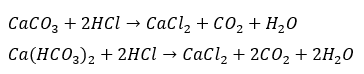
炭酸水素カルシウムについて・・・
これは、炭酸カルシウムに二酸化炭素を加えればいいだけです。
炭酸カルシウムが二酸化炭素と水とで合体するだけと覚えましょう。
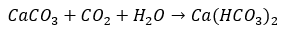
炭酸カルシウムについて・・・
炭酸カルシウムは作り方としては二つあります。
- 水酸化カルシウム水に二酸化炭素を吹き込む (理科の実験)
- 炭酸水素カルシウムの加熱分解

カルシウムと日常生活
カルシウムが日常生活のどのような部分で応用されているかをまとめます。
高校化学で覚えておくべきものは以下の3つです。
- サラシ粉・・・アニリン(有機)や漂白剤の検出
- 石膏/焼き石膏・・・美術の像とかに使われてる
- 塩化カルシウム・・・乾燥剤や融雪剤に
それぞれの化学式を紹介します。

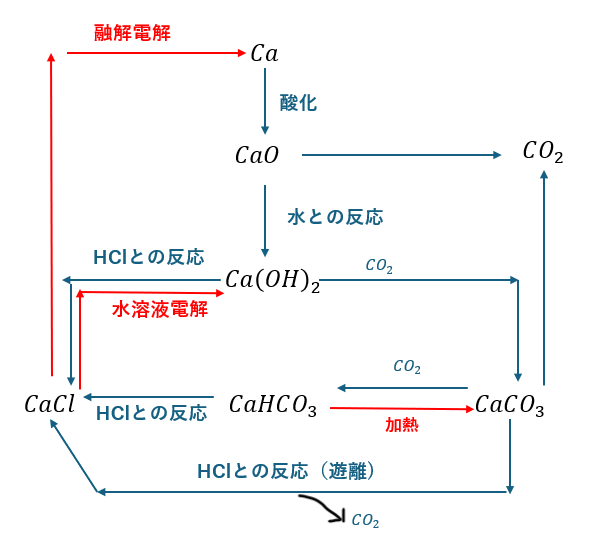
まとめ
カルシウムとその化合物についてまとめます。



コメント