こんにちは。Horyです。
前回の記事ではアルコールの性質や脱水について例え話を用いて解説しました。
今回の記事ではアルコールの酸化について原理から解説すると共に、級数による生成物の違いについて解説します。
今回も頑張りましょう。
前回の復習
アルコールの酸化について話す前に前回の記事の復習を行います。
まず、有機化学は酸化・還元の定義は以下のように示されます。
- 酸化・・・水素を失うこと
- 還元・・・水素を得ること
また、有機化合物の結合の強さについては・・・
- 電気陰性度
- H (のび太)・・・2.1
- C (スネ夫)・・・2.5
- O (ジャイアン)・・・3.5
- 反応性・・・「O-H > O-C > C-H」
- O-H・・・ジャイアンがのび太の電子を無理矢理奪う・・・関係切れやすい
- O-C・・・ジャイアンがスネ夫の電子を無理矢理借りた・・・関係はギスギス
- C-H・・・スネ夫がのび太から電子を借りてる・・・関係はそんなに悪くない
C-H結合もO-H結合も単結合(σ結合)で非常に硬いですが・・・
過マンガン酸カリウムや二クロム酸カリウム等の非常に強い酸化剤を用いれば切ることができます。
アルコールの酸化
先ほど説明したアルコール酸化のプロセスを図で説明します。
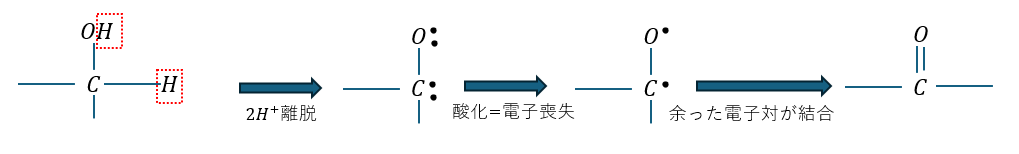
上に示すようにアルコールは酸化するとカルボニル結合を持った有機化合物になります。
カルボニル結合と言えば、アルデヒドかケトンですよね。
一級アルコールの酸化
一級アルコールは酸化されます。
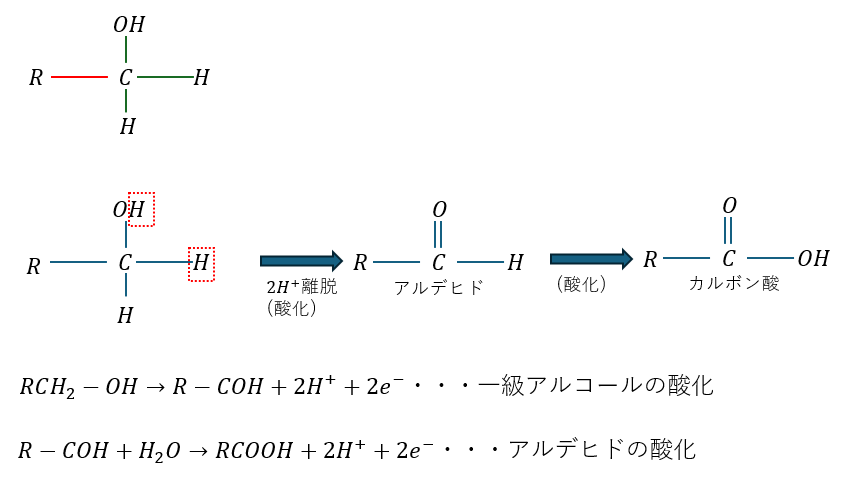
- 緑線・・・切りやすい結合
- 赤線・・・切りにくい結合
- 切りやすい結合が多い→酸化が進む
上の図でアルコールとアルデヒドは還元剤として反応しています。
半反応式についてはこちらの記事に書かれていますが、アルコールとアルデヒドの還元剤の式は覚えといた方が良いです(たまに出ます)。
- アルデヒド・・・中性
- カルボン酸・・・酸性
二級アルコールの酸化
二級アルコールは酸化されます。
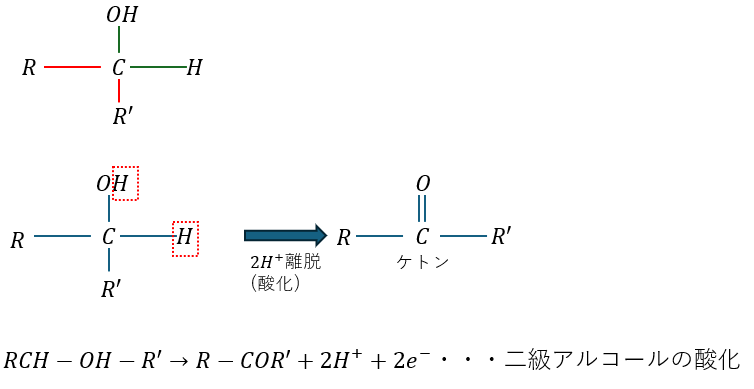
- 緑線・・・切りやすい結合
- 赤線・・・切りにくい結合
- 切りやすい/切りにくいが同じ→酸化が進む
上の図でアルコールは還元剤として反応しています。
- ケトン・・・中性
三級アルコールの酸化
三級アルコールは酸化されません。
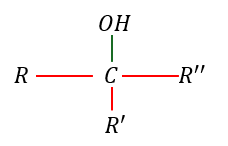
- 緑線・・・切りやすい結合
- 赤線・・・切りにくい結合
- 切りにくい結合が多い→酸化が進まない


コメント